Tartalom
Fő különbség
A fehérjék másodlagos épületén elhelyezett motívum szabályos, mint tekercselt vagy spirális jobb oldali megerősítés, amely egy spirál kiválóságát adja, ennek a ténynek köszönhetően, amelyet általában alfa-hélix néven ismertek. Alternatív megoldásként a béta-redős lemezt, amelyet gyakran b-lapnak is nevezünk, a fehérjékben jelen levő másodlagos épület standard motívumának vázoljuk.
Összehasonlító táblázat
| bázis | Alpha Helix | Beta redőzött lap |
| Meghatározás | A fehérjék másodlagos építésén elhelyezett motívum szabályos formává válik tekercselt vagy spirális jobb oldali megerősítésként, amely megadja a spirál kiválóságát. | A béta-redős lemezt, amelyet gyakran b-lapnak is nevezünk, a fehérjékben jelen levő másodlagos épület standard motívumának vázoljuk. |
| Aminosavak | Az aminosavak -R csoportjai a földön vannak. | Az -R csoportok vannak a lap padlóján és belső talajában. |
| kötődés | A hidrogénkötések az egész polipeptidláncon keresztül létrejönnek, hogy spirális szerkezeteket hozzanak létre. | A hidrogénkötésekből kettő vagy kétnél jobb béta-szál összekapcsolásával létezhet. |
Mi az Alpha Helix?
A fehérjék másodlagos épületén elhelyezett motívum szabályos, mint tekercselt vagy spirális jobb oldali megerősítés, amely egy spirál kiválóságát adja, ennek a ténynek köszönhetően, amelyet általában alfa-hélix néven ismertek. Az N-H csoport a fejlesztés során az egész hidrogénkötést jelöli a C = O csoporthoz, amelyet gyakran az aminosavak gerincének hívnak, amely négy aminosavban jelenik meg hamarabb, mint a fehérje szekvencia. A mai α-hélix demonstrálásának két kulcsfontosságú fejleménye volt: a kötésgeometria válása az aminosavak és peptidek drága kőépítési ítéletei és Pauling elvárása szerint a síkbeli peptidkötések miatt; és feladta annak a gyanúját, hogy létfontosságú számú lerakódás fordul elő a spirális csúszóján. A kritikus perc itt 1948 kora tavaszán szerezte meg magát, amikor Pauling itt egy hibával megszerezte a matracot. Kimerültséggel rajzolott egy normál korrekcióval rendelkező polipeptidláncot egy kis papírra, és egyenesen egy spirálba összecsukta, ügyelve arra, hogy vigyázzon a síkbeli peptidkötésekre. Az alfa-hélix alapvetően a természetben a legismertebb hélix-áram. Egy sebes polipeptidláncból áll, amelynek egészében az aminosavak oldalsó lánca kiszélesedik a középpontból, ez lehetővé teszi a típusának gondozását. Meglehetősen sokféle fehérjében is jelen lehetnek, például a globuláris fehérjéktől, például a mioglobintól a keratinig, amely egy vastag fehérje. Mindegyik lehet privilegizált vagy bal oldali helice, de bizonyosan bebizonyosodott, hogy az alfa-hélix hurok az oldalsó láncok eredményeként nem küzd. Ez az ismeret biztosítja az alfa-hélix stabilitását. Az alfa-hélix göndör mindegyik flip-jéhez három,6 aminosav-korrozív lerakódás van.
Mi az a Beta redős lap?
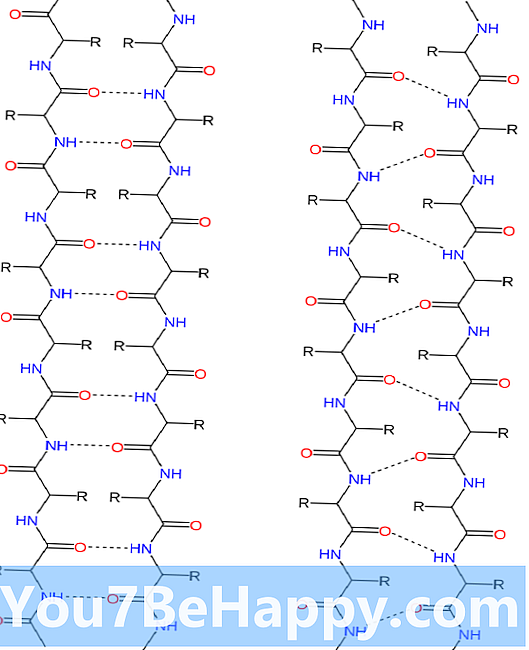
A béta-redős lemezt, amelyet gyakran b-lapnak is nevezünk, a fehérjékben jelen levő másodlagos épület standard motívumának vázoljuk. A teljesen különbözõ fehérjékkel szembeni megkülönböztetés az a nehézség, hogy olyan szálakból áll, amelyeknek legalább két vagy három hidrogénatomja vonatkozik a fejlesztés során, amely rendezi a redõsített lemezt. A β-szál olyan polipeptidhorgony, amely általában három-tíz aminosavat tartalmaz, a gerincvel meghosszabbítva, kibővített adaptációban. A β-lemezek szupramolekuláris kapcsolata a fehérjeösszegek és fibrillák összekapcsolódása során meglehetősen kevés emberi betegségben, azaz az amyloidózisban mutatkozik be, mint például az Alzheimer-betegség. Ez az épület akkor fordul elő, amikor a polipeptidlánc két alkotóeleme összehúzódik, és gépi hidrogénkötéseket ír be egymással. Ez a mozgás párhuzamos mozgási tervben vagy a párhuzamos terv ellenségeként fordulhat elő. Az egyenértékű sporttervvel párhuzamosan és annak irányában a polipeptidlánc irányultságának gyors következménye. A béta-gyűrött lap megfelelő épülete az α-gyűrött lap. Ez az épület lelkesen sokkal kevésbé végleges, mint a béta-gyűrött lap, és valóban példa nélküli a fehérjékben. Az α-gyűrött lemezt a karbonil- és aminocsoport összekapcsolódásával írják le; a karbonilcsoportokat összesen egyetlen fejezetben állítják be, míg az összes N-H gyűrűt alternatív módszerrel igazítják.
Főbb különbségek
- A fehérjék másodlagos épületén elhelyezett motívum szabályos, mint tekercselt vagy spirális jobb oldali megerősítés, amely egy spirál kiválóságát adja, ennek a ténynek köszönhetően, amelyet általában alfa-hélix néven ismertek. Alternatív megoldásként a béta-redős lemezt, amelyet gyakran b-lapnak is nevezünk, a fehérjékben jelen levő másodlagos épület standard motívumának vázoljuk.
- Az aminosavak -R csoportjai a hélix földfelszínén vannak, míg az -R csoportok a lap padlóján és belső talajában vannak.
- Az alfa-hélix egy polipeptidlánc, amelyet pólusformálnak és rugószerű épületben tekercselnek, hidrogénkötések tartják. Alternatív megoldásként a béta-redős lapok béta szálból készülnek, amelyek az oldal mellett vannak egymással összekötve legalább két hidrogénkötéssel, amelyek gerincét képezik.
- Hélix lehet balkezes (béta) vagy jobbkezes is, ahol az alfa-hélix állandóan jobb. Alternatív megoldásként a láncokat az alternatívát követõen 1-re állítják be, és egy másik, az alternatívát fordítva rendezett húrra béta-redõzött lapokban.
- Az alfa-hélix kialakulása oly módon létezik, hogy a hidrogénkötések a polipeptidláncon keresztül létrejönnek, hogy spirális konstrukciókat hozzanak létre. Alternatív megoldásként a béta-redős lapok úgy léteznek, hogy a hidrogénkötésekből kettő vagy kétnél jobb béta-szálat kötnek össze.

